摘要:這一發(fā)現(xiàn)可能會導(dǎo)致針對心血管疾病的更有針對性的治療方法。
美國國立衛(wèi)生研究院(NIH)的科學(xué)家們在了解“壞”膽固醇或低密度脂蛋白膽固醇(LDL-C)在體內(nèi)積累背后的機制方面取得了一個重要的里程碑成果。研究人員首次證明了低密度脂蛋白中的主要結(jié)構(gòu)蛋白如何與其受體相互作用,從而啟動低密度脂蛋白從血液中清除的過程。他們還確定了這一過程中斷的后果。
發(fā)表在《自然》雜志上的這一研究發(fā)現(xiàn),增強了我們對低密度脂蛋白如何導(dǎo)致心臟病的認識。心臟病是世界范圍內(nèi)死亡的主要原因,并可能為更有針對性的低密度脂蛋白降低療法鋪平道路,比如個性化的他汀類藥物治療,以提高其有效性。
 圖1
低密度脂蛋白受體結(jié)合的載脂蛋白B100的結(jié)構(gòu)
圖1
低密度脂蛋白受體結(jié)合的載脂蛋白B100的結(jié)構(gòu)低密度脂蛋白與心血管疾病之間的聯(lián)系
“低密度脂蛋白是心血管疾病的主要驅(qū)動因素之一,每33秒就有一人死亡,所以如果你想了解你的敵人,你想知道它是什么樣子的,”Alan Remaley醫(yī)學(xué)博士說,他是該研究的資深作者之一。
到目前為止,科學(xué)家們還無法可視化低密度脂蛋白的結(jié)構(gòu),特別是當(dāng)它與受體(一種被稱為LDLR的蛋白質(zhì))連接時會發(fā)生什么。通常,當(dāng)LDL與LDLR結(jié)合時,從血液中清除LDL的過程就開始了。但基因突變會阻止這種作用,導(dǎo)致低密度脂蛋白在血液中積聚,并以斑塊的形式沉積在動脈中,從而導(dǎo)致動脈粥樣硬化,這是心臟病的前兆。
在這項新研究中,研究人員使用高端技術(shù)來了解在該過程的關(guān)鍵階段發(fā)生了什么,并從新的角度看待低密度脂蛋白。
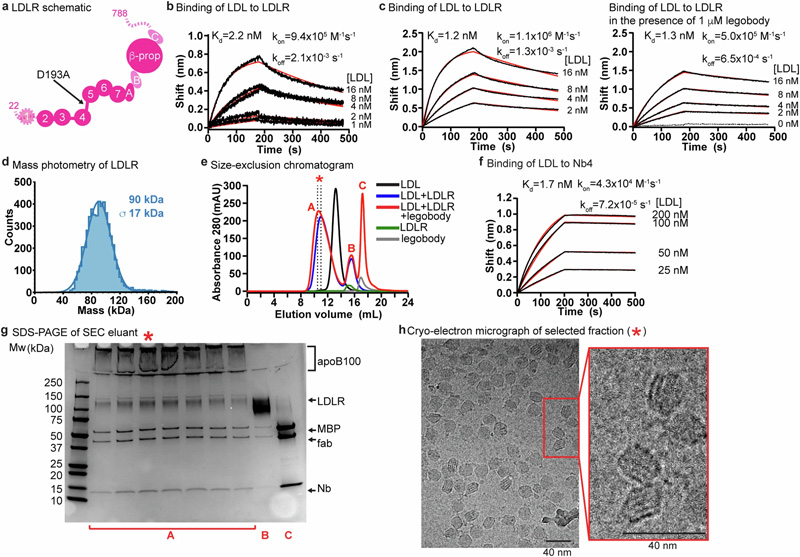
圖2 LDL、LDLR和legobody的生化特征
美國國立衛(wèi)生研究院國家過敏和傳染病研究所傳染病實驗室結(jié)構(gòu)病毒學(xué)科主任Joseph Marcotrigiano博士解釋說:“低密度脂蛋白體積巨大,大小不一,使其非常復(fù)雜。從來沒有人達到過我們這樣的分辨率。我們可以看到如此多的細節(jié),并開始揭示它在體內(nèi)是如何工作的”。
先進的技術(shù)揭示新的見解
利用稱為冷凍電子顯微鏡的先進成像技術(shù),研究人員能夠看到低密度脂蛋白與低密度脂蛋白結(jié)合時的結(jié)構(gòu)蛋白的整體。然后,利用人工智能驅(qū)動的蛋白質(zhì)預(yù)測軟件,他們能夠?qū)Y(jié)構(gòu)進行建模,并找到導(dǎo)致低密度脂蛋白增加的已知基因突變。該軟件的開發(fā)人員沒有參與這項研究,但他們最近獲得了2024年諾貝爾化學(xué)獎。
研究人員發(fā)現(xiàn),許多與低密度脂蛋白和低密度脂蛋白連接位置有關(guān)的突變與一種被稱為家族性高膽固醇血癥(FH)的遺傳性疾病有關(guān)。FH的特點是身體在細胞中吸收低密度脂蛋白的過程中存在缺陷,患有FH的人體內(nèi)的低密度脂蛋白水平極高,很可能在很小的時候就患上心臟病。他們發(fā)現(xiàn)fh相關(guān)的變異傾向于聚集在LDL的特定區(qū)域。
這項研究結(jié)果可能為開發(fā)靶向治療開辟新的途徑,旨在糾正這些由突變引起的功能失調(diào)的相互作用。但同樣重要的是,研究人員說,他們也可以幫助那些沒有基因突變,但膽固醇高且服用他汀類藥物的人,他汀類藥物通過增加細胞中的低密度脂蛋白來降低低密度脂蛋白。研究人員說,通過精確地了解低密度脂蛋白與低密度脂蛋白結(jié)合的位置和方式,他們現(xiàn)在可以針對這些連接點設(shè)計降低血液中低密度脂蛋白的新藥。
參考資料
[1] Structure of apolipoprotein B100 bound to the low-density lipoprotein receptor
摘要:這一發(fā)現(xiàn)可能會導(dǎo)致針對心血管疾病的更有針對性的治療方法。
美國國立衛(wèi)生研究院(NIH)的科學(xué)家們在了解“壞”膽固醇或低密度脂蛋白膽固醇(LDL-C)在體內(nèi)積累背后的機制方面取得了一個重要的里程碑成果。研究人員首次證明了低密度脂蛋白中的主要結(jié)構(gòu)蛋白如何與其受體相互作用,從而啟動低密度脂蛋白從血液中清除的過程。他們還確定了這一過程中斷的后果。
發(fā)表在《自然》雜志上的這一研究發(fā)現(xiàn),增強了我們對低密度脂蛋白如何導(dǎo)致心臟病的認識。心臟病是世界范圍內(nèi)死亡的主要原因,并可能為更有針對性的低密度脂蛋白降低療法鋪平道路,比如個性化的他汀類藥物治療,以提高其有效性。
 圖1
低密度脂蛋白受體結(jié)合的載脂蛋白B100的結(jié)構(gòu)
圖1
低密度脂蛋白受體結(jié)合的載脂蛋白B100的結(jié)構(gòu)低密度脂蛋白與心血管疾病之間的聯(lián)系
“低密度脂蛋白是心血管疾病的主要驅(qū)動因素之一,每33秒就有一人死亡,所以如果你想了解你的敵人,你想知道它是什么樣子的,”Alan Remaley醫(yī)學(xué)博士說,他是該研究的資深作者之一。
到目前為止,科學(xué)家們還無法可視化低密度脂蛋白的結(jié)構(gòu),特別是當(dāng)它與受體(一種被稱為LDLR的蛋白質(zhì))連接時會發(fā)生什么。通常,當(dāng)LDL與LDLR結(jié)合時,從血液中清除LDL的過程就開始了。但基因突變會阻止這種作用,導(dǎo)致低密度脂蛋白在血液中積聚,并以斑塊的形式沉積在動脈中,從而導(dǎo)致動脈粥樣硬化,這是心臟病的前兆。
在這項新研究中,研究人員使用高端技術(shù)來了解在該過程的關(guān)鍵階段發(fā)生了什么,并從新的角度看待低密度脂蛋白。

圖2 LDL、LDLR和legobody的生化特征
美國國立衛(wèi)生研究院國家過敏和傳染病研究所傳染病實驗室結(jié)構(gòu)病毒學(xué)科主任Joseph Marcotrigiano博士解釋說:“低密度脂蛋白體積巨大,大小不一,使其非常復(fù)雜。從來沒有人達到過我們這樣的分辨率。我們可以看到如此多的細節(jié),并開始揭示它在體內(nèi)是如何工作的”。
先進的技術(shù)揭示新的見解
利用稱為冷凍電子顯微鏡的先進成像技術(shù),研究人員能夠看到低密度脂蛋白與低密度脂蛋白結(jié)合時的結(jié)構(gòu)蛋白的整體。然后,利用人工智能驅(qū)動的蛋白質(zhì)預(yù)測軟件,他們能夠?qū)Y(jié)構(gòu)進行建模,并找到導(dǎo)致低密度脂蛋白增加的已知基因突變。該軟件的開發(fā)人員沒有參與這項研究,但他們最近獲得了2024年諾貝爾化學(xué)獎。
研究人員發(fā)現(xiàn),許多與低密度脂蛋白和低密度脂蛋白連接位置有關(guān)的突變與一種被稱為家族性高膽固醇血癥(FH)的遺傳性疾病有關(guān)。FH的特點是身體在細胞中吸收低密度脂蛋白的過程中存在缺陷,患有FH的人體內(nèi)的低密度脂蛋白水平極高,很可能在很小的時候就患上心臟病。他們發(fā)現(xiàn)fh相關(guān)的變異傾向于聚集在LDL的特定區(qū)域。
這項研究結(jié)果可能為開發(fā)靶向治療開辟新的途徑,旨在糾正這些由突變引起的功能失調(diào)的相互作用。但同樣重要的是,研究人員說,他們也可以幫助那些沒有基因突變,但膽固醇高且服用他汀類藥物的人,他汀類藥物通過增加細胞中的低密度脂蛋白來降低低密度脂蛋白。研究人員說,通過精確地了解低密度脂蛋白與低密度脂蛋白結(jié)合的位置和方式,他們現(xiàn)在可以針對這些連接點設(shè)計降低血液中低密度脂蛋白的新藥。
參考資料
[1] Structure of apolipoprotein B100 bound to the low-density lipoprotein receptor



