麻省理工學(xué)院麥戈文腦研究所的科學(xué)家們通過(guò)對(duì)秀麗隱桿線蟲(Caenorhabditis elegans)的研究,揭開了一個(gè)長(zhǎng)期存在的謎團(tuán),即控制細(xì)胞凋亡的因素:一種能夠防止程序性細(xì)胞死亡的蛋白質(zhì)是如何促進(jìn)細(xì)胞程序性死亡的。上個(gè)月,秀麗隱桿線蟲第四次獲得了諾貝爾獎(jiǎng)。他們的研究由麻省理工學(xué)院David H. Koch生物學(xué)教授Robert Horvitz領(lǐng)導(dǎo),并于10月9日在《Science Advances》雜志上發(fā)表,揭示了健康和疾病中細(xì)胞死亡的過(guò)程。
疼痛信號(hào)新見解:一種鈣通道蛋白起關(guān)鍵作用
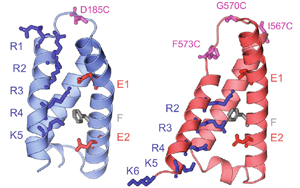
在目前的研究中,Link?ping大學(xué)的研究人員專注于一種名為CaV2.2的鈣通道,它與疼痛信號(hào)的傳遞有關(guān)。事實(shí)上,這些通道在慢性疼痛時(shí)更加活躍。它們特別位于感覺(jué)神經(jīng)細(xì)胞的末端。
Science:首次發(fā)現(xiàn)谷氨酰胺代謝開關(guān)是紅細(xì)胞發(fā)育的關(guān)鍵
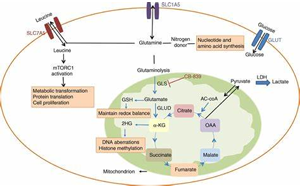
造血干細(xì)胞經(jīng)過(guò)不同的階段發(fā)育為完全成熟的紅細(xì)胞。這一基本的生物過(guò)程是由一系列復(fù)雜的代謝過(guò)程決定的。在鐮狀細(xì)胞病和β-地中海貧血等血液疾病中,這些過(guò)程往往失調(diào)。近日,美國(guó)圣裘德兒童醫(yī)院的科學(xué)家們首次發(fā)現(xiàn)了谷氨酰胺在這一過(guò)程中的作用。研究表明,調(diào)節(jié)谷氨酰胺代謝有望治療常見的紅細(xì)胞疾病。同時(shí),谷氨酰胺的豐度可以作為評(píng)估療效的工具。
EGFR基因突變,基因編輯技術(shù)揭示癌癥耐藥性途徑
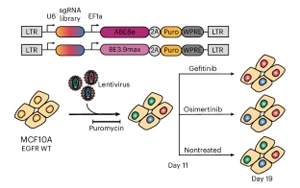
在最近發(fā)表在《自然生物技術(shù)》(Nature Biotechnology)雜志上的一項(xiàng)研究中,瑞士的研究人員使用堿基和引物編輯技術(shù),在多種細(xì)胞系(包括癌細(xì)胞和非癌細(xì)胞)中創(chuàng)建和分析了上皮生長(zhǎng)因子受體(EGFR)基因的各種變體,以研究它們對(duì)癌癥進(jìn)展和耐藥性的影響。他們發(fā)現(xiàn),以前已知的和新的突變都與EGFR激活和藥物反應(yīng)顯著相關(guān),證明了該方法的準(zhǔn)確性,并揭示了影響腫瘤生長(zhǎng)和耐藥性機(jī)制的新途徑。
科學(xué)家發(fā)現(xiàn)了阿爾茨海默病檢測(cè)和治療的腦脊液標(biāo)志物
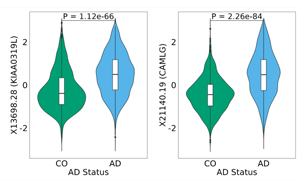
在最近發(fā)表在《Nature Genetics》上的一項(xiàng)研究中,研究人員調(diào)查了人類腦脊液(CSF)蛋白質(zhì)組的基因組特征。通過(guò)探索腦脊液蛋白的遺傳藍(lán)圖,這項(xiàng)研究發(fā)現(xiàn)了新的標(biāo)記物和治療靶點(diǎn),可能會(huì)在阿爾茨海默病的診斷和護(hù)理方面取得進(jìn)展。
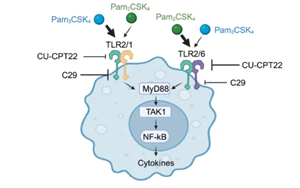
突破性方法揭示了免疫受體如何檢測(cè)感染
免疫細(xì)胞能夠像嗅探犬一樣檢測(cè)感染,使用一種叫做Toll樣受體的特殊傳感器,簡(jiǎn)稱TLRs。但是是什么信號(hào)激活了TLRs,這種激活的規(guī)模和性質(zhì)與被檢測(cè)到的物質(zhì)之間有什么關(guān)系?在最近的一項(xiàng)研究中,來(lái)自波恩大學(xué)和波恩大學(xué)醫(yī)院(UKB)的研究人員使用了一種創(chuàng)新的方法來(lái)回答這些問(wèn)題。他們采用的方法可能有助于加快尋找對(duì)抗傳染病、癌癥、糖尿病或癡呆癥的藥物。

突變蛋白在一些致命癌癥中的新作用
美國(guó)國(guó)立衛(wèi)生研究院(NIH)的科學(xué)家和合作者表示,他們發(fā)現(xiàn)了一種新的途徑,即RAS基因(在癌癥中常見的突變)可能會(huì)推動(dòng)腫瘤生長(zhǎng),而不是在細(xì)胞表面發(fā)揮眾所周知的信號(hào)傳導(dǎo)作用。RAS基因是癌癥中第二常見的突變基因,突變的RAS蛋白是一些最致命癌癥的關(guān)鍵驅(qū)動(dòng)因素。
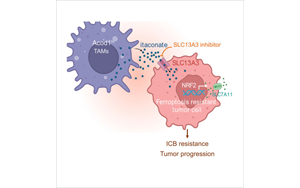
Cancer Cell發(fā)現(xiàn)了一些癌癥對(duì)免疫治療沒(méi)有反應(yīng)的關(guān)鍵原因:代謝機(jī)制阻礙免疫反應(yīng)
密歇根大學(xué)Rogel癌癥中心的研究人員發(fā)現(xiàn)了一些癌癥對(duì)免疫治療沒(méi)有反應(yīng)的關(guān)鍵原因:腫瘤微環(huán)境中的代謝物轉(zhuǎn)運(yùn)體阻斷了免疫反應(yīng)不可或缺的一種關(guān)鍵類型的腫瘤細(xì)胞死亡。
《Nature》腸道中的某些大腸桿菌如何促進(jìn)結(jié)腸癌?
科學(xué)家已經(jīng)發(fā)現(xiàn)腸道中的某些大腸桿菌是如何通過(guò)與腸細(xì)胞結(jié)合并釋放一種破壞dna的毒素來(lái)促進(jìn)結(jié)腸癌的發(fā)生的。這項(xiàng)發(fā)表在《Nature》雜志上的研究揭示了一種潛在降低癌癥風(fēng)險(xiǎn)的新方法。這項(xiàng)研究是由Lars Vereecke教授(VIB-UGent炎癥研究中心)和Han Remaut教授(VIB-VUB結(jié)構(gòu)生物學(xué)中心)的團(tuán)隊(duì)進(jìn)行的。




